【佳文荐读】基于中国背景的细菌耐药所致健康和经济负担的系统评价
日期:2021-11-09 作者:周越,杨瑶瑶,张翕,胡琳,杜可欣,郑波,管晓东,海沙尔江·吾守尔,史录文 来源:《中国药房》2021年20期


中文核心期刊
中国科技核心期刊
中国科技论文统计源期刊
RCCSE中国核心学术期刊
《中国学术期刊影响因子年报》统计源期刊
《国家科技期刊开放平台》收录期刊
中国期刊方正双效期刊
第三届国家期刊奖获奖期刊
第一届重庆市政府出版奖获奖期刊
CA、AJ、IPA、WPRIM、UPD、JST收录期刊
CMCC、CMCI、CJFD、CBMdisc收录期刊
纪念新中国成立70周年重庆市品牌期刊
重庆市出版专项资金资助期刊
国家卫生健康委员会主管
中国医院协会 重庆大学附属肿瘤医院主办
ISSN 1001-0408
CN 50-1055/R
CODEN ZYHAA4
日期:2021-11-09 作者:周越,杨瑶瑶,张翕,胡琳,杜可欣,郑波,管晓东,海沙尔江·吾守尔,史录文 来源:《中国药房》2021年20期
编者按:为深入学习贯彻习近平新时代中国特色社会主义思想,落实2021年全国宣传部长会议和全国卫生健康工作会议精神,聚焦中国共产党成立以来卫生健康事业历史进程中的重要决策、活动及成果,从不同角度和层面展现卫生健康事业发展的重要成就。“中国药房立体网络平台暨药事服务系统”“系统”特开设了“党为人民谋健康的100年”新媒体主题宣传专栏,涉及时事新闻、原创大众健康类科普文章、人文药学、期刊佳文荐读等与我国健康卫生事业与药学工作相关的宣传文章,从而助力提高人民健康水平制度保障、坚持和发展中国特色卫生健康制度。本篇文章《基于中国背 景的细菌耐药所致健康和经济负担的系统评价》在细菌耐药持续发展的背景下,通过收集文献对我国细菌耐药的健康和经济负担 情况、测算方法以及研究质量进行汇总、分析,以期为我国细菌耐药负担的测算研究提供科学依据,为国家遏制细菌耐药的政策制 定提供参考。
基于中国背景的细菌耐药所致健康和经济负担的系统评价
周越,杨瑶瑶,张翕,胡琳,杜可欣,郑波,管晓东,海沙尔江·吾守尔,史录文
摘 要 目的:为我国细菌耐药所致负担的测算研究提供科学依据,为国家遏制细菌耐药的政策制定提供参考。方法:计算机检 索中国知网、万方数据、维普网、PubMed、Scopus、Medline和EconoLite等数据库,收集基于中国背景的细菌耐药负担的相关研究, 检索文献的发表时间为2016年1月1日-2020年8月10日。经独立筛选文献、提取资料后,采用Newcastle-Ottawa(NOS)量表进 行文献质量评价,对细菌耐药造成的健康和经济负担进行描述性分析。结果:共纳入中英文文献27篇。纳入文献的NOS评分为 4~6分,均采用回顾性病例对照设计,将患者分为病例组(耐药菌感染)和对照组(敏感菌感染或无感染),研究常用测算指标包括 死亡率、住院时长和诊治费用。纳入的研究中,耐药菌感染者的死亡率是敏感菌感染者的0.7~12.0倍,其总住院时长的平均值或 中位数是敏感菌感染者的0.9~2.5倍,其总诊治费用的平均值或中位数是敏感菌感染者的1.0~2.7倍。上述指标在耐药菌感染者 和无感染者之间的差异更大。结论:细菌耐药会增加患者的健康和经济负担。但现有相关文献质量中等,以单中心研究为主,样 本代表性不足,研究设计未考虑时间依赖性偏倚且可重复性低,研究指标较单一,测算范围较局限,亟需开展更高质量、多中心的 实证调查以全面测算我国细菌耐药所致的健康和经济负担。
细菌耐药已成为全球关注的卫生健康领域焦点,也是当今世界面临的最紧迫的公共卫生问题之一。细菌耐药会增加患者感染机会,加重其临床症状,延长住院时间,增加医疗卫生资源消耗。相比敏感菌感染,耐药菌感染会增加更多的死亡和患病概率以及治疗成 本[1-2]。有文献报道,以当前的发展趋势,到2050 年,全 球将有1000万人死于细菌耐药,且全球因细菌耐药造 成的累计成本将达到100万亿美元[2]。可见,科学测算细菌耐药负担、合理配置医疗资源,已成为各国遏制细菌耐药的重要抓手之一。
目前已有部分研究对细菌耐药带来的健康和经济负担的相关研究方法、结果及质量进行了综述[1-3],然而尚缺乏基于我国背景的相关文献综述。为了解我国细菌耐药所致健康和经济负担的测算研究情况,本课题组拟通过收集文献,分析我国细菌耐药的健康和经济负担情况、测算方法以及研究质量,以期为我国细菌耐药负担的测算研究提供科学依据,为国家遏制细菌耐药的政 策制定提供参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 纳入标准 本研究的纳入标准包括:(1)中文和 英文论著;(2)研究数据来自中国;(3)任何研究设计类 型的原始研究;(4)研究对象为人类。
1.1.2 排除标准 本研究的排除标准包括:(1)评论、通 信、病例汇报、会议摘要、综述等文献;(2)研究内容与细 菌耐药无关的文献;(3)研究病原菌为寄生虫、真菌、结 核分枝杆菌、艾滋病毒、流感病毒等的文献;(4)未评价 细菌耐药负担的文献;(5)不包含对照组(敏感菌感染或 无感染)的文献。
1.1.3 研究对象 细菌感染的患者,不包括结核分枝杆 菌感染患者。
1.1.4 测算指标 测算指标包括死亡率、住院时长和诊 治费用。
1.2 文献检索策略
文献检索策略由本课题组成员共同商定。计算机检 索中国知网、万方数据、维普网、PubMed、Scopus、Medline 和EconoLite等数据库,收集细菌耐药负担的相关研究, 检索文献的发表时间为2016年1月1日-2020年8月10 日。中文检索词为“抗菌药物”“耐药”“负担”“死亡率”等; 英文检索词为“antibiotic”“resistance”“burden“”mortality” 等。以PubMed为例,文献检索策略如图1所示。

1.3 文献筛选与资料提取
文献筛选和资料提取分别由本文第一和第二作者独立开展,完成后由这两位作者对纳入文献和提取资料进行交叉核对,意见不一致时征求本文通信作者的意见。使用 EndNote 8.0 文献管理工具,依次通过阅读题目、摘要和全文进行文献筛选,剔除不符合纳入标准的文献。完成筛选后,使用Excel 2019对纳入文献进行资料提取。提取资料包括:第一作者、发表时间、题目、研究时长、研究类型与设计、研究指标、研究结果等。
1.4 文献质量评价
研究采用Newcastle-Ottawa(NOS)量表评价队列和病例对照研究的质量[3]。NOS量表分别从病例组和对照组的定义与选择、病例组与对照组的可比性和暴露的确定等3个方面进行评分。满分为9分,本研究设定评分≥7分为高质量研究、4~6分为中等质量研究、≤3分为低质量研究。
1.5 数据处理
本研究采用Excel 2019软件统计文献发表情况并对纳入的研究进行描述性系统评价。
2 结果
2.1 文献检索结果和纳入研究的基本情况
初检共获得相关文献12 391篇,依据文献题目和摘要筛选纳入125篇;依据全文筛选,最终纳入27篇[4-30]。文献筛选流程及结果如图2所示。
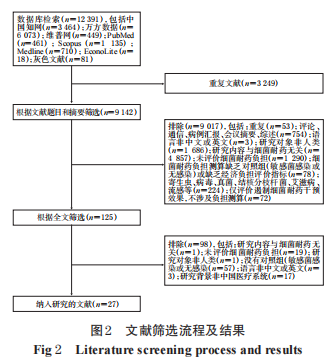
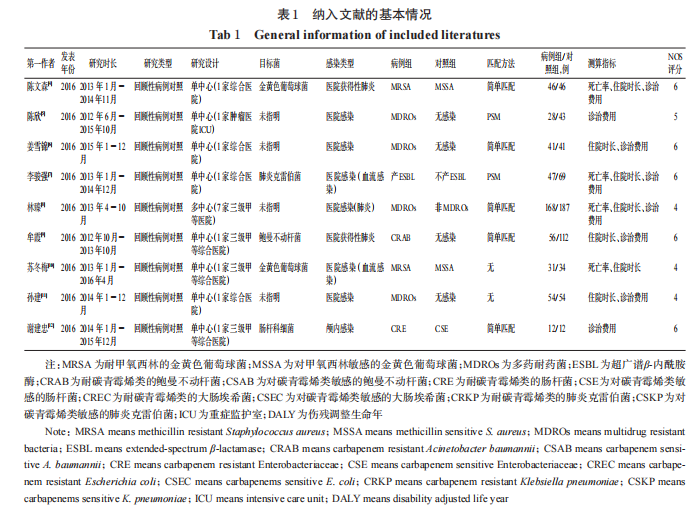
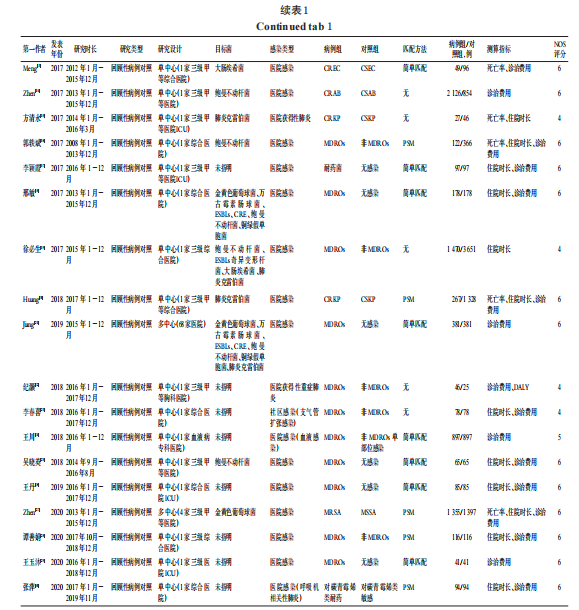
所有纳入的研究均为回顾性病例对照研究,病例组为耐药菌感染,对照组为敏感菌感染或无感染。其中, 有13项研究依据患者年龄、性别、诊断等变量为病例组匹配对照组[4,6,8-9,12-13,17-18,21,24-26,29],7项研究采用倾向评分匹配(PSM)法匹配病例组和对照组[5,7,16,20,27-28,30]。研究以单中心为主,仅3项研究为多中心研究[8,21,27]。除1项研究的患者感染类型为社区感染(支气管扩张感染) 外[23],其余研究均为医院感染。研究对象感染类型以血流感染[7,10]、肺炎[4,8-9,15,22,30]等为主。测算指标包括死亡率[4,7-8,10,13,15-16,20,27]、住院时长[4,6-11,15-20,23,25-28,30]和诊治费用[4-9,11-14,16-18,20-30]等。所有研究的NOS评分为4~6分,均为中等质量研究。纳入文献的基本情况见表1。
2.2 细菌耐药所致的健康负担
纳入文献中,9 项研究汇报了耐药菌感染的死亡率[4,7-8,10,13,15-16,20,27]( 表2)。
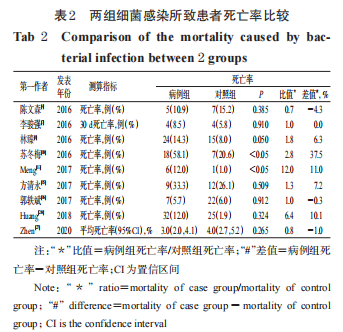
6项研究的结果显示,耐药菌感染者的死亡率是敏感菌感染者的1.0~6.4倍[7-8,10,15-16,20], 2项研究得出耐药菌感染与敏感菌感染者死亡率比较差异有统计学意义(P<0.05)[10,13],且 Meng 等[13]测算结果显示,CREC 感染组患者的死亡率为 CSEC 组的 12.0 倍。该研究的患者特征信息显示,相比于CSEC感染组,CREC 感染组住院时长>6 个月、ICU 住院时长>6 个 月、有手术/尿道插管/机械通气/气管切开/纤维支气管镜检查/中心静脉置管/置胃管/伤口引流等情况的患者占比更高。由于CREC感染组患者自身身体状况更差,可能进一步增加其死亡风险,从而导致CREC感染组死亡率远高于CSEC感染组。19 项研究汇报了总住院时长[4,6-11,15-20,23,25-28,30] (表 3),其中4项研究汇报了感染后住院时长[4,7,10,15],1项研究汇报了ICU住院时长[15]。除3项研究两组患者的住院时长比较差异无统计学意义(P>0.05)[4,10,15]外,其余研究均显示耐药菌感染组患者的住院时长显著长于对照组(P<0.05 或 P<0.01 或 P<0.001)[6-9,11,16-20,23,25-28,30]。
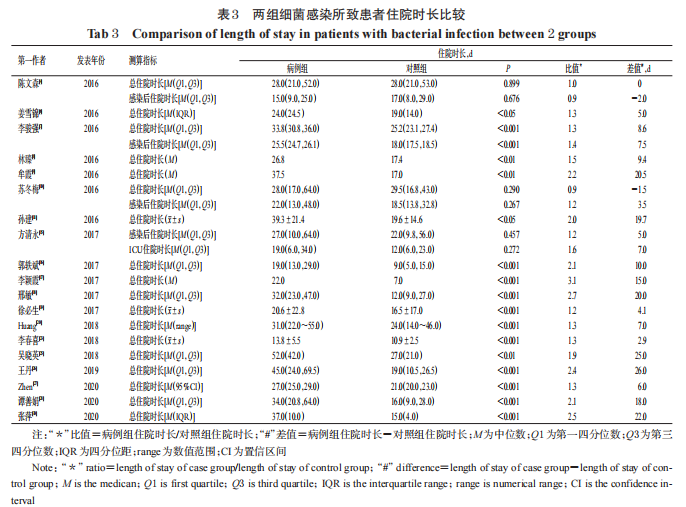
耐药菌感染者总住院时长的平均值或中位数是敏感菌感染者的0.9~2.5倍,两者总住院时长的平均值或中位数之差为-1.5~22.0 d[4,7,10,15,20,27,30]。MDROs 感染者总住院时长的平均值或中位数是非 MDROs 感染者的1.2~2.1倍,两者总住院时长的平均值或中位数之差是2.9~18.0 d[8,16,19,23,28]。此外,耐药菌感染者总住院时长的平均值或中位数是无感染者的1.3~3.1倍,两者总住院时长的中位数之差为5.0~26.0 d[6,9,11,17-18,25-26]。可见,耐药菌感染者与无感染住院者时长之差相较于耐药菌感染者与敏感菌感染者的住院时长之差更大。另有 1 项研究比较了 MDROs 感染对比非 MDROs感染患者的 DALY,结果发现,MDROs 感染组为(3.4± 5.7)DALYs,显著长于非 MDROs 感染组的(0.7±2.4)DALYs(P<0.01)[22]。
2.3 细菌耐药所致经济负担
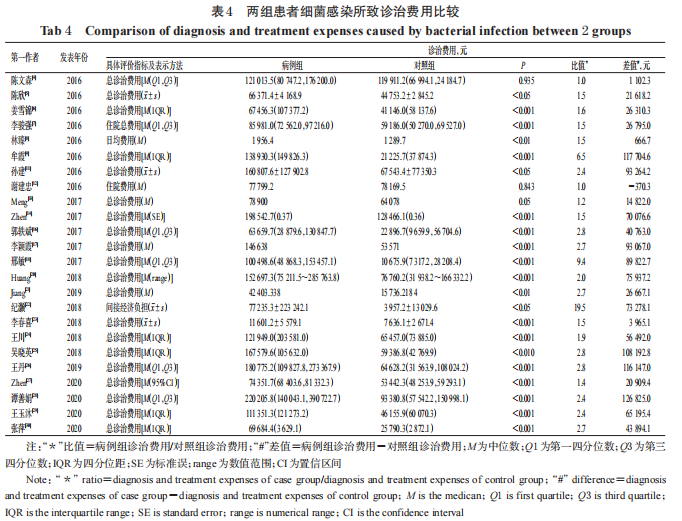
24 项研究汇报了细菌耐药感染的诊治费用(表 4)[4-9,11-14,16-18,20-30]。除3项研究两组患者的诊治费用比较差异无统计学意义(P>0.05 或 P=0.05)[4,12-13]外,其余研究均显示耐药菌感染组患者的诊治费用显著高于对照组(P<0.05或P<0.01或P<0.001)[4-9,11,14,16-18,20-30]。由纳入文献可知,耐药菌感染者总诊治费用的平均值或中位数是敏感菌感染者的1.0~2.7倍,两者总诊治费用的平均值或中位数之差为-370.3~75 937.2元[4,7,12-14,20,27,30];MDROS 感染者总诊治费用的平均值或中位数是非MDROS 感染的 1.5~2.8 倍,两者总诊治费用的平均值或中位数之差为3 965.1~126 825.0元[16,23-24,28];耐药菌或 MDROS 感染者总诊治费用的平均值或中位数是无感染者的1.5~9.4倍,总诊治费用的平均值或中位数之差为 21 618.2~117 704.6 元[5-6,9,11,17-18,21,25-26,29]。可见,耐药菌感染意味着需要花费更多的总诊治费用,加重了患者的经济负担。此外,由表4还可以看出,绝大部分纳入研究对于费用负担的测算仅汇报了总费用,尚缺乏对于感染后诊治费用的分析和测算。
3 讨论
耐药菌感染是当今世界共同面临的严重的公共卫生问题之一,严重威胁着人类健康。本研究以中国为背景,综合评价细菌耐药带来的健康和经济负担,结果发现耐药菌感染将显著延长或增加患者的住院时长和总诊治费用。
3.1 耐药菌感染可增加患者健康负担
耐药菌感染通常被认为会加重患者的临床症状、增加其死亡风险。一项基于发展中国家的系统综述发现,耐药菌感染患者具有更高的死亡率[31]。而本研究纳入的27篇文献中仅有2篇文献的结果显示,耐药菌感染患者的死亡率与敏感菌感染患者比较,差异有统计学意义[10,13]。这可能是因为我国相关研究多以单中心为主,研究时长较短、患者样本量较小,从而降低了病例组和对照组的死亡率差异,最终导致两组差异无统计学意义。住院时长是从医院角度评价耐药菌感染负担的重要指标之一。通常情况下,耐药菌感染会延长患者治疗时间,增加住院时长。本研究纳入的部分文献结果显示,病例组患者的住院时长显著长于对照组[6-9,11,16-20,23,25-28,30]。然而,耐药菌感染是疾病进展过程中的一种状态(即暴露),并非一种疾病诊断,患者病程本身会随着时间变化而发生改变。因此,相关研究采用的经典病例对照研究设计可能忽略了患者住院时长对结局的影响,可能高估了病例组与对照组患者总住院时长的差别[32]。同时,本研究也发现,纳入文献并未测算耐药菌感染导致患者住院时长变化的具体值,这可能导致业界对细菌耐药所致医疗资源消耗的认识存在偏差。
3.2 耐药菌感染可增加患者经济负担
除1项研究外[12],其余研究病例组患者的总诊治费用均大于对照组[4-6,9,11,13-14,16-18,20-21,23-30]。耐药菌感染患者,尤其是MDROS感染的患者,其身体状况往往更差,具有更高的被收入ICU治疗的风险,且需要使用更多的抗菌药物。因此,耐药菌感染患者的诊治费用通常会高于敏感菌感染或无感染患者。谢建忠等[12]研究发现,虽然颅内 CRE 感染组患者的每床日住院费用显著高于颅 内 CSE 感染组患者(7 008.82 元 vs.2 777.75 元,P< 0.05),但是两组总住院费用没有明显差别(77 799.2 元vs.78 169.5元,P>0.05)。这可能是因为颅内CRE感染患者具有较高的死亡率从而导致其住院时长缩短、总住院费用相对减少,但每床日住院费用还是显著高于颅内CSE感染组患者。因此可以推测,颅内CRE感染可直接导致患者经济负担加重;此外还可以推测,由于患者伤残、死亡所导致的间接经济损失将远远超过CSE感染。
3.3 现有研究的不足与改进
建议基于对纳入文献的分析以及NOS量表评价结果,本研究发现现有文献在数据来源、研究设计、研究可重复性和研究指标等4个方面仍存在较大的提升空间。
3.3.1 单中心研究为主,样本代表性不足 由纳入文献可知,目前基于中国背景的研究大多仅收集了单家医院的数据,且样本医院多为三级甲等医院,患者样本量较小(纳入研究中病例组样本量中位数为78例,对照组样本量中位数为94例),制约了结果的代表性。为实现对我国细菌耐药所致健康和经济负担的全面测算,今后研究仍需结合细菌耐药的临床特点、不同级别医疗机构特点等相关因素,制定科学严谨的样本遴选方案,开展多中心研究,以全面反映我国细菌耐药所致负担情况。
3.3.2 研究设计未考虑时间依赖性偏倚 现有研究均为基于病例对照的传统研究设计。虽然部分研究试图采用简单匹配或PSM等方法确定病例组和对照组,以缩小两组患者的基线特征差异,然而由于感染是一种疾病进展过程,该研究方法忽略了住院时长对患者结局的影响,研究结果的科学性和严谨性仍待商榷。因此,未来研究应充分考虑到细菌耐药的特殊性,尝试采用多状态模型等国际推荐方法对患者住院时长和医疗费用进行测算比较,以降低时间依赖性偏倚的影响[33]。
3.3.3 研究可重复性低 现有研究对数据收集、清洗与统计分析的汇报大多较为模糊,制约了研究的可重复性和科学性。为实现对研究结果的准确解读和二次文献分析(如 Meta 分析),未来研究需更为详细地汇报评价方法,以提高结果的科学性。
3.3.4 研究指标较单一,测算范围较局限 现有文献大多分析了病例组与对照组患者死亡率、住院时长和总住院费用的差异,尚无研究测算两组相关指标的具体差值。此外,现有文献的研究指标也较少,主要集中在临床结局、诊疗费用等指标,且测算范围局限,未能充分考虑到细菌耐药造成的直接非医疗成本和间接成本,如看护费用、劳动力损失等的影响,故结果可能低估了细菌耐药的负担。Maragakis等[34]指出,在分析细菌耐药所致经济负担时,主要涉及4类成本——住院成本(抗菌药物治疗、住院时间延长、ICU 住院时间、诊断检查、医护人员人力)、门诊成本(医师人力、抗菌药物治疗、随访和康复中心)、患者成本(生产力损失和旅途花费)和社会成本(抗菌药物效力下降)等。建议今后研究能够以此为基础,纳入更多指标,全面测算细菌耐药所致负担,从而提高测算结果的准确性。
3.4 本研究的局限性
本研究存在如下局限性:(1)纳入文献对研究指标的汇报方式存在差异(中位数或平均值),无法进行Meta分析,导致无法获得定量分析结果。(2)纳入的文献均为回顾性研究。相较于前瞻性多中心研究,回顾性研究可能存在数据缺失以及选择偏倚的问题,进而影响本研究结果的可信度。(3)大部分研究都是单中心研究,且主要从患者和医院角度出发评价细菌耐药所致负担,未能考虑到细菌耐药对于社会层面的影响,如劳动力损失等,因此本文可能低估了耐药菌感染导致的实际负担。
综上所述,本研究综合梳理了现有的文献证据,分析了我国耐药菌感染所致的健康和经济负担。然而,现有研究总体质量中等,研究类型较为局限,所选测算指标较少且样本量较小,同时受数据可获得性的影响,研究多为单中心研究且研究数量尚且不足,亟需开展更高质量、多中心的实证调查以全面测算我国细菌耐药所致的健康和经济负担,以期为我国制定细菌耐药相关政策提供科学依据。
参考文献
[ 1 ] NAYLOR N R,ATUN R,ZHU N,et al. Estimating the burden of antimicrobial resistance:a systematic literature review[J]. Antimicrob Resist Infect Control,2018,7(1):58.
[ 2 ] ZHEN X,LUNDBORG C S,SUN X,et al. Economic burden of antibiotic resistance in ESKAPE organisms:a systematic review[J]. Antimicrob Resist Infect Control,2019, 8(1):137.
[ 3 ] GA Wells,B Shea,D O’Connell,et al. The NewcastleOttawa scale(NOS)for assessing the quality of nonrandomised studies in meta-analyses[EB/OL]. [2020-11-24].http://www.ohri.ca/programs/clinical_epidemiology/oxford.asp.
[ 4 ] 陈文森,李松琴,李慧芬,等.倾向指数配比分析(PSM):MRSA与MSSA医院获得性肺炎预后比较[J].中国感染控制杂志,2016,15(5):299-303.
[ 5 ] 陈欣.重症住院患者并发医院感染对医疗费用的影响[J].预防医学,2016,28(8):835-837. [ 6 ] 姜雪锦,孙吉花,邢敏,等.综合医院感染多药耐药菌特点及直接经济损失分析[J].中华医院感染学杂志,2016,26(24):5727-5729.
[ 7 ] 李骏强,汤陈琪,王慧,等.肺炎克雷伯菌是否产超广谱β-内酰胺酶对血流感染患者临床结局及医疗成本的影响[J].中华医学杂志,2016,96(24):1903-1906.
[ 8 ] 林臻,黄倩倩,王萍,等.多药耐药菌感染肺炎直接的经济损失调查[J].中华医院感染学杂志,2016,26(15):3577-3579.
[ 9 ] 牟霞,张满,杨廷秀,等.耐碳青霉烯类鲍氏不动杆菌医院获得性肺炎的经济负担[J].中华医院感染学杂志,2016,26(18):4274-4276.
[10] 苏冬梅,黄燕,刘一,等.耐甲氧西林金黄色葡萄球菌血流感染的临床特征及易感因素分析[J].实用医学杂志,2016,32(20):3412-3415.
[11] 孙建.多药耐药菌医院感染对患者住院日和住院费用的影响[J].中华医院感染学杂志,2016,26(18):4277-4279.
[12] 谢建忠,黄勋.颅内碳青酶烯类耐药与敏感肠杆菌科细菌感染的治疗及其经济学损失分析[J].中华医院感染学杂志,2016,26(18):4271-4273.
[13] MENG X,LIU S,DUAN J,et al. Risk factors and medical costs for healthcare-associated carbapenem-resistant Escherichia coli infection among hospitalized patients in aChinese teaching hospital[J]. BMC Infect Dis,2017,17(1):82.
[14] ZHEN X,CHEN Y,HU X,et al. The difference in medical costs between carbapenem-resistant Acinetobacter baumannii and non-resistant groups:a case study from a hospital in Zhejiang province,China[J]. Eur J Clin Microbiol Infect Dis,2017,36(10):1989-1994.
[15] 方清永. ICU中CRKP感染的医院获得性肺炎患者耐药及预后的危险因素分析[D].重庆:重庆医科大学,2017.
[16] 郭轶斌.多药耐药与非耐药鲍曼不动杆菌院内感染的归因住院费用与住院时长研究[J].中国卫生统计,2017,34(3):378-381.
[17] 李颖霞. ICU住院患者耐药菌感染监测及直接经济负担研究[D].济南:山东大学,2017.
[18] 邢敏.连续3年多重耐药菌医院感染监测与经济负担评价[J].中国消毒学杂志,2017,34(11):1045-1047.
[19] 徐必生,袁华兵,杨萍.某三级综合医院多重耐药菌相关感染经济负担评估[J/OL].中华实验和临床感染病杂志(电子版),2017,11(5):455-459[2017-11-03]. http://doi.10.3877/cma.j.issn.1674-1358.2017.05.006.
[20] HUANG W,QIAO F,ZHANG Y,et al. In-hospital medical costs of infections caused by carbapenem-resistant Klebsiellapneumoniae[J]. Clin Infect Dis,2018,67(suppl 2):s225-s230.
[21] JIANG H,LI W,HOU T,et al. The attributable direct medical cost of healthcare associated infection caused by multidrug resistance organisms in 68 hospitals of China[J/OL]. Biomed Res Int,2019:1-7[2019-03-05].http://pubmed.ncbi.nlm.nih.gov/30949509/. DOI:10.1155/2019/7634528.
[22] 纪灏.应用DALY结合人力资本法研究某三甲专科医院医院获得性重症肺炎的间接经济负担[J].中国感染控制杂志,2018,17(12):1055-1059.
[23] 李春喜,韩明锋,周晓平,等.支气管扩张伴感染患者病原菌分布及耐药致直接经济损失研究[J].临床肺科杂志,2018,23(9):1680-1683.
[24] 王川,陈琳,王津雨,等.血液病患者医院感染所致直接经济损失[J].中国感染控制杂志,2018,17(10):923-927.
[25] 吴晓英,丁丽娜,吴修建.多重耐药鲍曼不动杆菌医院感染的直接经济损失研究[J].中国感染控制杂志,2018,17(8):735-738.
[26] 王丹.综合ICU住院患者多重耐药菌医院感染与经济负担[J].中国感染控制杂志,2019,18(7):648-653. [27] ZHEN X,LUNDBORG C S,ZHANG M,et al. Clinical and economic impact of methicillin-resistant Staphylococcus aureus:a multicentre study in China[J]. Sci Rep,2020,10(1):3900.
[28] 谭善娟.某三级医院ICU多重耐药菌医院感染经济负担研究[J].中国感染控制杂志,2020,19(6):564-568.
[29] 王玉沐,汪爱兰,黄锡华. ICU多重耐药菌医院感染情况及直接经济负担评价[J].当代临床医刊,2020,33(3):297-298.
[30] 张萍.呼吸机相关性肺炎碳青霉烯类抗菌药物耐药菌感染经济损失[J].中华医院感染学杂志,2020,30(6):856-860.
[31] FOUNOU R C,FOUNOU L L,ESSACK S Y. Clinical and economic impact of antibiotic resistance in developing countries:a systematic review and meta-analysis[J].PLoS One,2017,12(12):e0189621.
[32] HAWKEY P M. The growing burden of antimicrobial resistance[J]. J Antimicrob Chemother,2008,62(suppl 1):s1-s9. [33] MACEDO-VI?AS M,DE ANGELIS G,ROHNER P,et al. Burden of meticillin-resistant Staphylococcus aureus infections at a Swiss University Hospital:excess length of stay and costs[J]. J Hosp Infect,2013,84(2):132-137. [34] MARAGAKIS L L,PERENCEVICH E N,COSGROVE SE. Clinical and economic burden of antimicrobial resistance[J]. Expert Rev Anti Infect Ther,2008,6(5):751-763.
Δ 基金项目:国家自然科学基金国际(地区)合作与交流项目(No. 81861138048);国家自然科学基金面上项目(No. 81973294);美国中华医学基金会资助项目(No. 17-270)
第一作者简介
周越,博士研究生。研究方向:细菌耐药负担测算。电话:010-82805019。E-mail:zhouyuezhy@pku.edu.cn
通信作者简介
海沙尔江·吾守尔,助理研究员,博士。研究方向:抗菌药物合理使用与细菌耐药负担测算。电话:010-82805019。E-mail:kaiser@bjmu.edu.cn
编校:刘钰
审核:邹小勇